Rượu etylic, một hợp chất hữu cơ quen thuộc, đóng vai trò quan trọng trong chương trình Hóa học lớp 9. Bài 34 sẽ giúp các em hiểu rõ về tính chất, ứng dụng và điều chế của loại rượu này. Trong bài viết này, BaDaoVl sẽ cung cấp lời giải chi tiết cho các bài tập trong sách giáo khoa, kèm theo những kiến thức bổ trợ, giúp các em nắm vững nội dung bài học.
Rượu etylic, hay còn được gọi là etanol, có công thức hóa học là C2H5OH. Nó là một chất lỏng không màu, dễ bay hơi, có mùi thơm đặc trưng và vị cay. Trong đời sống, rượu etylic được sử dụng rộng rãi trong nhiều lĩnh vực, từ sản xuất đồ uống có cồn đến ứng dụng trong công nghiệp. Việc tìm hiểu về rượu etylic không chỉ giúp các em đạt điểm cao trong môn Hóa học mà còn trang bị kiến thức hữu ích cho cuộc sống.
Tính chất vật lý của rượu etylic
Rượu etylic là chất lỏng không màu, tan vô hạn trong nước, nhẹ hơn nước và sôi ở nhiệt độ 78,3 độ C. Tính chất vật lý này ảnh hưởng đến cách sử dụng và bảo quản rượu etylic.
Độ tan của rượu etylic
Rượu etylic tan vô hạn trong nước nhờ khả năng tạo liên kết hydro với phân tử nước. Điều này giải thích tại sao rượu etylic thường được sử dụng để pha chế đồ uống.
Tính chất hóa học của rượu etylic
Rượu etylic có thể tham gia vào nhiều phản ứng hóa học quan trọng, bao gồm phản ứng cháy, phản ứng với natri và phản ứng este hóa.
Phản ứng cháy của rượu etylic
Rượu etylic cháy trong không khí tạo ra khí cacbonic và nước, đồng thời tỏa nhiều nhiệt. Phản ứng này được biểu diễn bằng phương trình hóa học: C2H5OH + 3O2 → 2CO2 + 3H2O.
Phản ứng của rượu etylic với natri
Khi cho natri vào rượu etylic, sẽ xảy ra phản ứng tạo ra khí hydro và natri etylat. Phản ứng này được sử dụng để nhận biết rượu.
Điều chế rượu etylic
Rượu etylic được điều chế bằng phương pháp lên men tinh bột hoặc đường. Quá trình này diễn ra nhờ hoạt động của các vi sinh vật, chủ yếu là nấm men.
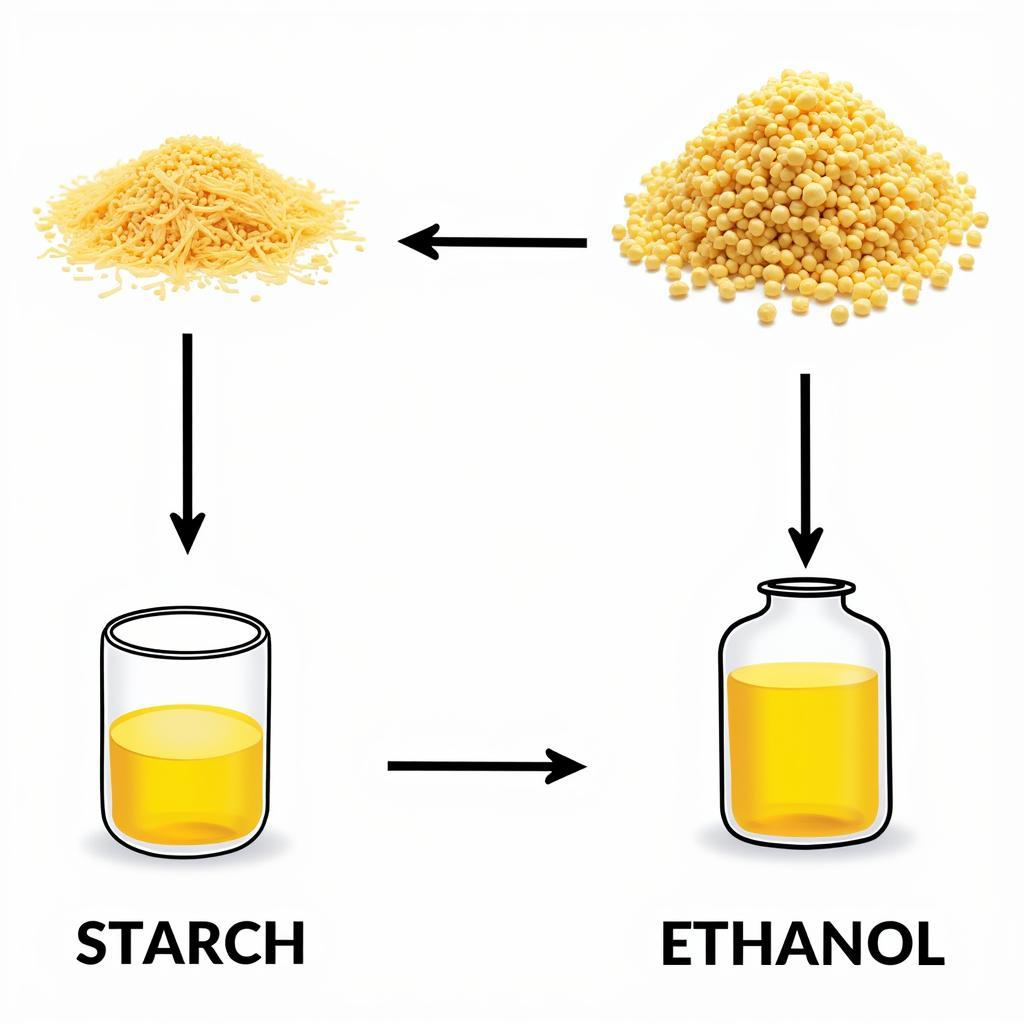 Lên men tinh bột
Lên men tinh bột
Giải bài tập Hóa 9 bài 34
BaDaoVl cung cấp lời giải chi tiết cho các bài tập trong sách giáo khoa Hóa học 9 bài 34, giúp các em hiểu rõ hơn về tính chất và ứng dụng của rượu etylic.
giải bài tập hóa 8 oxi không khí
Bài tập 1
Hãy viết phương trình hóa học của phản ứng cháy của rượu etylic.
Đáp án: C2H5OH + 3O2 → 2CO2 + 3H2O
giải bài tập 8 bài 1 vật lý 11
Kết luận
Bài 34 về rượu etylic cung cấp cho học sinh lớp 9 những kiến thức quan trọng về một hợp chất hữu cơ phổ biến. Hiểu rõ về tính chất, ứng dụng và điều chế của rượu etylic sẽ giúp các em vận dụng kiến thức vào thực tiễn và đạt kết quả tốt trong học tập. “Giải Bt Hóa Lớp 9 Bài 34” là một bước quan trọng giúp các em nắm vững kiến thức này.
bài tập giải toán lớp 2 trang 175
FAQ
- Rượu etylic có tan trong nước không? (Có, tan vô hạn)
- Công thức hóa học của rượu etylic là gì? (C2H5OH)
- Rượu etylic được điều chế bằng phương pháp nào? (Lên men tinh bột hoặc đường)
- Sản phẩm của phản ứng cháy của rượu etylic là gì? (Khí cacbonic và nước)
- Rượu etylic có tác dụng gì trong đời sống? (Sản xuất đồ uống, dùng trong công nghiệp,…)
- Khi cho natri vào rượu etylic sẽ tạo ra khí gì? (Khí hydro)
- Nhiệt độ sôi của rượu etylic là bao nhiêu? (78,3 độ C)
công thức giải nhanh bài tập adn
giải bài toán lớp 3 bằng 2 cách
Khi cần hỗ trợ hãy liên hệ Email: [email protected], địa chỉ: Tòa nhà Etown Central, 11 Đoàn Văn Bơ, Quận 4, TP. Hồ Chí Minh, Việt Nam.. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.