Giải bài tập hóa 9 sách giáo khoa bài 13 axit bazơ muối là chủ đề trọng tâm trong chương trình hóa học lớp 9. Bài viết này sẽ cung cấp lời giải chi tiết, dễ hiểu cho các bài tập trong sách giáo khoa hóa 9 bài 13, kèm theo những kiến thức bổ trợ giúp bạn nắm vững nội dung bài học.
Axit, Bazơ và Muối: Khái niệm cơ bản
Bài 13 hóa 9 tập trung vào ba loại hợp chất quan trọng: axit, bazơ và muối. Hiểu rõ khái niệm và tính chất của từng loại là chìa khóa để giải quyết các bài tập một cách hiệu quả. Axit là những hợp chất khi tan trong nước phân li ra ion H+. Bazơ là những hợp chất khi tan trong nước phân li ra ion OH-. Muối là hợp chất tạo thành khi thay thế một hay nhiều nguyên tử hidro trong phân tử axit bằng nguyên tử kim loại.
Giải Bài Tập Hóa 9 Sách Giáo Khoa Bai 13: Chi Tiết và Dễ Hiểu
Sách giáo khoa hóa 9 bài 13 bao gồm nhiều dạng bài tập từ cơ bản đến nâng cao, đòi hỏi học sinh vận dụng kiến thức về axit, bazơ và muối để giải quyết. Chúng ta sẽ cùng đi qua một số bài tập điển hình và phân tích cách giải.
Bài tập về nhận biết axit, bazơ và muối
Dạng bài tập này yêu cầu học sinh phân biệt các chất dựa vào công thức hóa học hoặc tính chất đặc trưng. Ví dụ, nhận biết các dung dịch HCl, NaOH, NaCl. Chúng ta có thể sử dụng quỳ tím để nhận biết: HCl làm quỳ tím chuyển đỏ (tính axit), NaOH làm quỳ tím chuyển xanh (tính bazơ), NaCl không làm đổi màu quỳ tím (tính trung tính).
 Nhận biết Axit, Bazơ và Muối bằng Quỳ Tím
Nhận biết Axit, Bazơ và Muối bằng Quỳ Tím
Bài tập về phản ứng giữa axit và bazơ
Phản ứng trung hòa giữa axit và bazơ tạo thành muối và nước là một trong những phản ứng quan trọng nhất trong hóa học. Ví dụ, viết phương trình phản ứng giữa HCl và NaOH. Phương trình phản ứng: HCl + NaOH → NaCl + H2O.
Bài tập về phản ứng giữa axit và kim loại
Một số kim loại phản ứng với axit tạo thành muối và giải phóng khí hidro. Ví dụ, viết phương trình phản ứng giữa Zn và HCl. Phương trình phản ứng: Zn + 2HCl → ZnCl2 + H2.
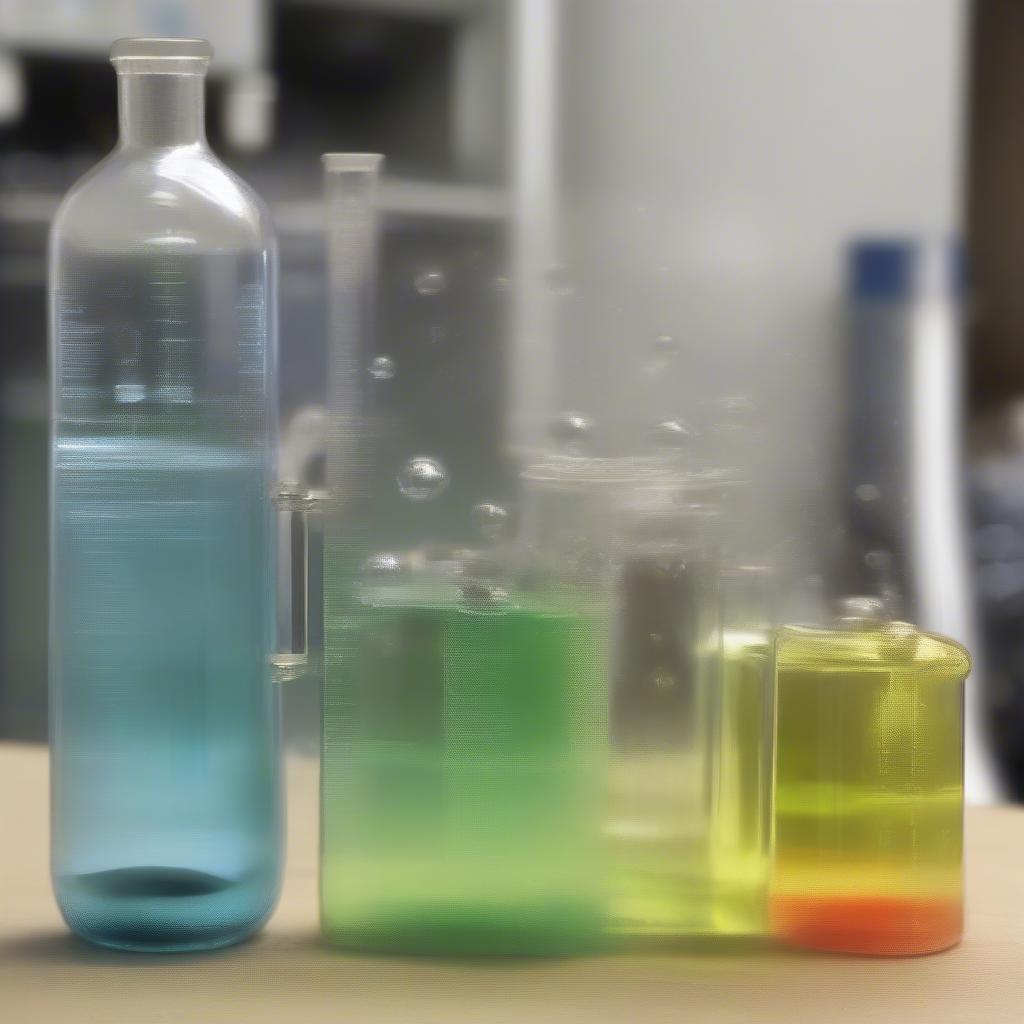 Phản ứng giữa Axit và Kim Loại
Phản ứng giữa Axit và Kim Loại
Bài tập về tính toán nồng độ dung dịch
Dạng bài tập này yêu cầu học sinh tính toán nồng độ mol, nồng độ phần trăm của dung dịch axit, bazơ hoặc muối. Để giải quyết, cần nắm vững công thức tính nồng độ và cách chuyển đổi giữa các đơn vị.
Theo PGS.TS Nguyễn Văn A, chuyên gia hóa học tại Đại học Khoa học Tự nhiên, “Việc nắm vững kiến thức về axit, bazơ và muối là nền tảng quan trọng cho việc học tập hóa học ở các cấp học cao hơn.”
Kết luận
Giải bài tập hóa 9 sách giáo khoa bài 13 axit bazơ muối không chỉ giúp bạn đạt điểm cao trong các bài kiểm tra mà còn củng cố kiến thức nền tảng cho việc học tập hóa học sau này. Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích và giúp bạn tự tin hơn trong việc giải quyết các bài tập hóa học.
FAQ
- Axit là gì?
- Bazơ là gì?
- Muối là gì?
- Phản ứng trung hòa là gì?
- Làm thế nào để nhận biết axit, bazơ và muối?
- Công thức tính nồng độ mol là gì?
- Công thức tính nồng độ phần trăm là gì?
 Công thức tính nồng độ dung dịch
Công thức tính nồng độ dung dịch
Mô tả các tình huống thường gặp câu hỏi về giải bài tập hóa 9 sách giáo khoa bai 13.
Học sinh thường gặp khó khăn trong việc phân biệt axit, bazơ và muối, viết phương trình phản ứng hóa học và tính toán nồng độ dung dịch.
Gợi ý các câu hỏi khác, bài viết khác có trong web.
Bạn có thể tìm hiểu thêm về các bài tập hóa học khác tại BaDaoVl.






