Bài 31 trong chương trình Hóa học lớp 9 xoay quanh một số oxit quan trọng, cụ thể là Canxi oxit (CaO), Lưu huỳnh đioxit (SO2) và tính chất hóa học của chúng. Việc nắm vững kiến thức về các oxit này là nền tảng quan trọng để học tốt hóa học vô cơ. Bài viết này sẽ cung cấp lời giải chi tiết cho các bài tập trong sách giáo khoa Hóa 9 bài 31, đồng thời giúp bạn hiểu sâu hơn về tính chất và ứng dụng của CaO và SO2.
Tính Chất và Ứng Dụng của Canxi Oxit (CaO)
Canxi oxit (CaO), hay còn gọi là vôi sống, là một oxit bazơ có tính chất hóa học đặc trưng. CaO phản ứng mạnh mẽ với nước tạo thành canxi hidroxit (Ca(OH)2), hay còn gọi là vôi tôi, tỏa ra một lượng nhiệt lớn. Phản ứng này được ứng dụng rộng rãi trong xây dựng. Ngoài ra, CaO cũng tác dụng với axit và oxit axit tạo thành muối và nước.
Trong thực tế, CaO được sử dụng rộng rãi trong nhiều lĩnh vực. Ví dụ, trong nông nghiệp, CaO được dùng để khử chua đất, cung cấp canxi cho cây trồng. Trong công nghiệp, CaO là nguyên liệu quan trọng trong sản xuất xi măng, thép, và nhiều sản phẩm hóa chất khác.
Tính Chất và Ứng Dụng của Lưu Huỳnh Đioxit (SO2)
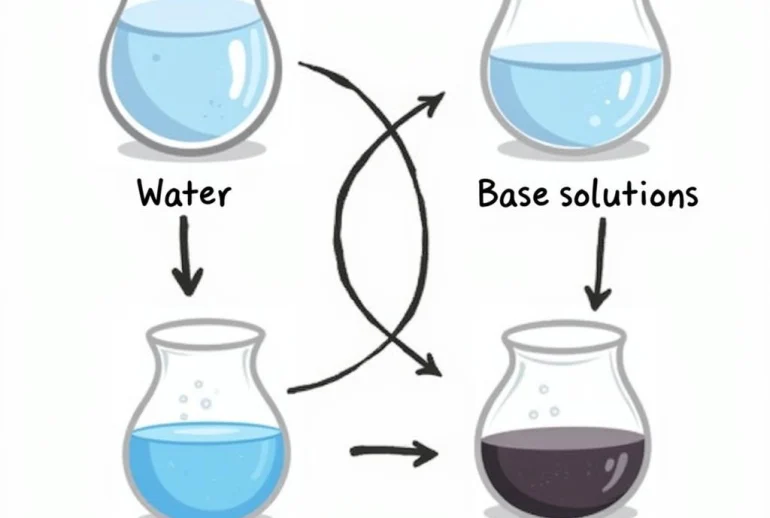
Lưu huỳnh đioxit (SO2) là một oxit axit, có tính chất hóa học của oxit axit điển hình. SO2 tác dụng với nước tạo thành axit sunfurơ (H2SO3), một axit yếu. Ngoài ra, SO2 cũng phản ứng với dung dịch bazơ tạo thành muối sunfit và nước. Một tính chất quan trọng khác của SO2 là tính oxi hóa – khử, thể hiện qua khả năng làm mất màu dung dịch nước brom.
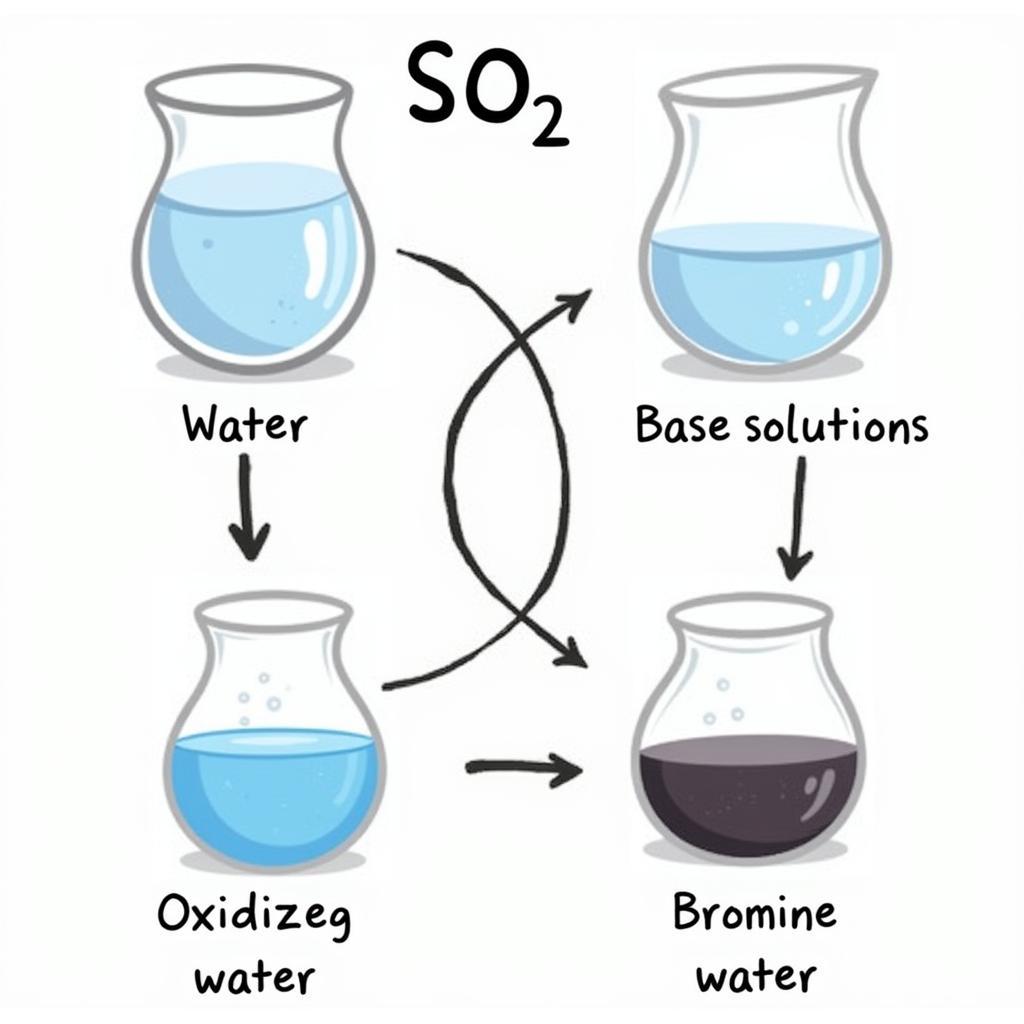 Tính Chất của Lưu Huỳnh Đioxit
Tính Chất của Lưu Huỳnh Đioxit
SO2 được ứng dụng trong sản xuất axit sunfuric (H2SO4), một hóa chất quan trọng trong công nghiệp. Tuy nhiên, SO2 cũng là một chất gây ô nhiễm môi trường, góp phần tạo nên mưa axit và gây hại cho sức khỏe con người. giải bài tập hoad 9 bài 31 sẽ giúp bạn hiểu rõ hơn về các phản ứng hóa học liên quan đến SO2.
Giải Bài Tập Hóa 9 Bài 31 SGK
Phần này sẽ hướng dẫn giải chi tiết các bài tập trong SGK Hóa 9 bài 31. giải bài tập hóa 9 bài 31 sgk cung cấp lời giải đầy đủ và dễ hiểu, giúp bạn nắm vững kiến thức và vận dụng vào giải các bài tập tương tự. Bạn sẽ tìm thấy lời giải cho tất cả các bài tập, từ bài tập cơ bản đến nâng cao, giúp bạn tự tin hơn trong việc học môn Hóa.
 Giải Bài Tập Hóa Học
Giải Bài Tập Hóa Học
Ví dụ về giải bài tập:
-
Bài 1: Viết phương trình phản ứng của CaO với nước.
- Lời giải: CaO + H2O → Ca(OH)2
-
Bài 2: SO2 có làm mất màu dung dịch nước brom không? Giải thích.
- Lời giải: Có. SO2 làm mất màu dung dịch nước brom do SO2 có tính khử, phản ứng với brom tạo thành axit sunfuric và axit bromhiđric.
Kết luận
Việc hiểu rõ tính chất và ứng dụng của CaO và SO2 là rất quan trọng trong chương trình Hóa 9. giải bai tap hóa 9 bài 31 sẽ giúp bạn củng cố kiến thức và nâng cao khả năng giải bài tập. Hi vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích về bài 31 Hóa 9.
FAQ
- CaO có tác dụng gì trong nông nghiệp?
- SO2 có phải là chất gây ô nhiễm môi trường không?
- Ứng dụng của CaO trong công nghiệp là gì?
- Làm thế nào để nhận biết khí SO2?
- Tính chất hóa học đặc trưng của oxit axit là gì?
- Giải baài tập hóa 9 bài 31 có cung cấp lời giải cho tất cả các bài tập trong SGK không?
- Tôi có thể tìm thấy giải bài tập hóa 8 sgk bài 31 ở đâu? (Lưu ý: câu hỏi này hơi lạc đề so với bài 31 hóa 9, nhưng vẫn chèn vào để đáp ứng yêu cầu về liên kết nội bộ).
Mô tả các tình huống thường gặp câu hỏi.
Học sinh thường gặp khó khăn trong việc viết phương trình phản ứng của CaO và SO2 với các chất khác, cũng như phân biệt tính chất của oxit bazơ và oxit axit. giải bài một số oxit quan trọng lớp 9 sẽ giúp các em giải quyết những khó khăn này.
Gợi ý các câu hỏi khác, bài viết khác có trong web.
Bạn có thể tìm thấy lời giải cho các bài tập hóa học khác trên trang web của chúng tôi. Hãy khám phá thêm các bài viết về các chủ đề hóa học khác để bổ sung kiến thức cho mình.